新型コロナウイルスを検出する「超高感度抗原検査法」を開発
発表のポイント
- 新型コロナウイルス感染症では、PCR検査が一般のクリニックではなかなか行えないため、その手法に代わる迅速で簡単に検査可能な「抗原検査」の普及が待ち望まれている
- これまでの抗原検査は検出感度の不足と検出ウイルスを上手く区別できないなどの問題があった
- 多くの実験室に備わっているマイクロプレートリーダーを使用し、特定の波長の光の吸収変化を測定するだけの、PCR検査より安価で簡易な手法を開発した
- 今後は実際の患者検体での測定を早急に実施し、約30分程度でのウイルス検出を目指す
早稲田大学(本部:東京都新宿区、総長:田中愛治)教育・総合科学学術院の伊藤悦朗教授の研究グループ(以下、同研究グループ)は、従来のPCR検査の手法を大幅に簡略化しウイルス検出感度も高い、新しい「超高感度抗原検査法(以下、新たな検査法)」の開発に成功しました。
新型コロナウイルス感染症の検査方法としては、遺伝子の特定を目的とするPCR検査、インフルエンザなどの罹患を調べる際に用いられる抗原検査、罹患経験の有無を調べる抗体検査、の大きく分けて3つの方法が存在します。従来の抗原検査は、検出感度の不足や、検出したコロナウイルスを新型か従前のものかを区別できない場合もあることからPCR検査に比べてあまり普及していません。一方でPCR検査も臨床検査技師による実施が必要であることや、結果が出るまで2日程度要すること、技術的な問題で偽陰性が出やすいことなどの理由から一般のクリニックではなかなか実施できないため、迅速で簡易、そして高い確率でウイルスを検出可能な、新しい抗原検査の普及が待ち望まれています。
そこで同研究グループは、抗原検査が抱える問題点を大幅に改善し、安価で簡易かつ感度の高い新たな検査法を開発しました。
新たな検査法には、同研究グループがこれまで取り組んできた極微量タンパク質の超高感度定量測定法を適用しました。マイクロプレートリーダーを活用し、特定の波長の光の吸収変化を測定するだけでウイルスを検出することができます。使用する試薬もPCR検査と比べはるかに安価となり、より高い感度で新型コロナウイルスを検出できます。
今後は、実際の患者検体での測定を早急に実施し、新しい検査方法が広く社会実装されることを目指します。
【論文情報】
雑誌名:Diagnostics
DOI:10.3390/diagnostics10080594
【研究助成】
研究費名:科学技術振興機構(JST) 研究成果最適展開支援プログラム(A-STEP)
研究課題名:高病原性鳥インフルエンザウイルスの迅速高感度検出システムの開発(JPMJTR184B)
研究代表者名(所属機関名):研究責任者 伊藤悦朗(早稲田大学)、プロジェクトリーダー(企業責任者) 太田俊也(株式会社タウンズ)
(1)これまでの研究で分かっていたこと
早稲田大学教育・総合科学学術院の伊藤悦朗教授の研究グループは、これまでに(株)タウンズ(本社:静岡県伊豆の国市、代表取締役社長:野中 雅貴)とともに、極微量タンパク質の超高感度定量測定法の開発に取り組んできました。この方法はELISA法(※1)と酵素サイクリング法(※2)とを組み合わせたユニークなものです。

(ELISA法に酵素サイクリング法を組み合わせることで、超高感度検出を可能にしました。)
この超高感度定量測定法を応用することで、2019年には、尿中ではほとんど検出不可能であるアディポネクチンとよばれるタンパク質の検出に成功し、慢性腎臓病の進行に伴って、尿中のアディポネクチン濃度が上昇することを見いだし、糖尿病の治療に新たな指針を与えることができました。
新型コロナウイルス感染症の検査方法としてはPCR検査が良く知られていますが、これは中核病院や保健所などでの実施が必要となり、町医者などの一般クリニックではなかなか行えないのが現状です。一般クリニックでは、その代わりとなる、迅速で簡単な「抗原検査」の利用が待望されています。しかし、これまでの抗原検査には大きな2つの問題があり、①検出感度が不足していること、ウイルスが検出できた場合でも、②そのウイルスが新型か従来型であるかの区別がしづらいこと、が難点でした。これら2点を解決するために、上記の超高感度定量測定法を新型コロナウイルスに適用し超高感度でタンパク質を検出することに成功しました。この超高感度定量測定法が新型コロナ感染症の抗原検査(すなわちタンパク質検査)として応用可能であることを見いだしたのです。
(2)今回の研究で新たに実現しようとしたこと、明らかになったこと
現在の新型コロナウイルス感染症の抗原検査には2つの課題があります。
1つ目の課題はウイルス検出感度の低さです。2020年5月のScience誌には「新型コロナウイルス感染症の抗原検査は早くて安いが、正確性に欠ける」(出典1)という記事が載りました。また4月の時点ですが、世界保健機構(WHO)も「抗原検査の開発は推し進めるべきであるが、まだ使用を推奨しない」(出典2)と発言していました。その検出感度を上げるために、開発した極微量タンパク質の超高感度定量測定法を適用しました。この方法ではマイクロプレートリーダーを活用し、迅速に、かつ、特定の波長の光の吸収変化を測定するだけで新型コロナウイルスを検出できます。これは比色法と呼ばれる検査方法で、一般クリニックでもすぐに実施できる測定方法です。基本的に臨床検査技師が行うPCR検査とは異なり、新たな検査法は医師や看護師でも実施でき、試薬もPCR検査で使用されているものと比べればはるかに安価です。PCR検査の場合2-3万円程度必要なところを、新たな検査法では2-3000円程度の費用に抑えることを目指しています。タンパク質の検出感度もアットモル(※3)レベルの超高感度での測定が可能です。通常は化学発光酵素免疫測定法(※4)という特別な装置を利用したときにのみ測定できる感度ですが、我々の方法では、光の吸光度を測るだけで特別な装置は必要としません。またタンパク質の数とRNA量とを換算してみると、この感度はPCR検査に肉薄するものだということも分かりました。
2つ目の課題は、検出されたウイルスが新型コロナウイルスなのか従来型のコロナウイルスなのかを区別しづらい点です。検出ウイルスの特異性と呼ばれるものですが、この特異性が低いと、検査を受けた患者が新型コロナウイルスに感染しているのか、その他のコロナウイルスに感染しているのかを区別することができません。
コロナウイルスの表面にはスパイクタンパク質と呼ばれる突起があります。このスパイクタンパク質がコロナ、すなわち王冠、のように見えるのでコロナウイルスと呼ばれています。このスパイクタンパク質が人の細胞の受容体に作用することで、ウイルスの体内への侵入が始まります。新たな検査法を活用し、このスパイクタンパク質に着目することで、新型と従来型のコロナウイルスを区別することができ、検出ウイルスの特異性が出せます。新型コロナウイルスのスパイクタンパク質を超高感度で検出することに成功しました。
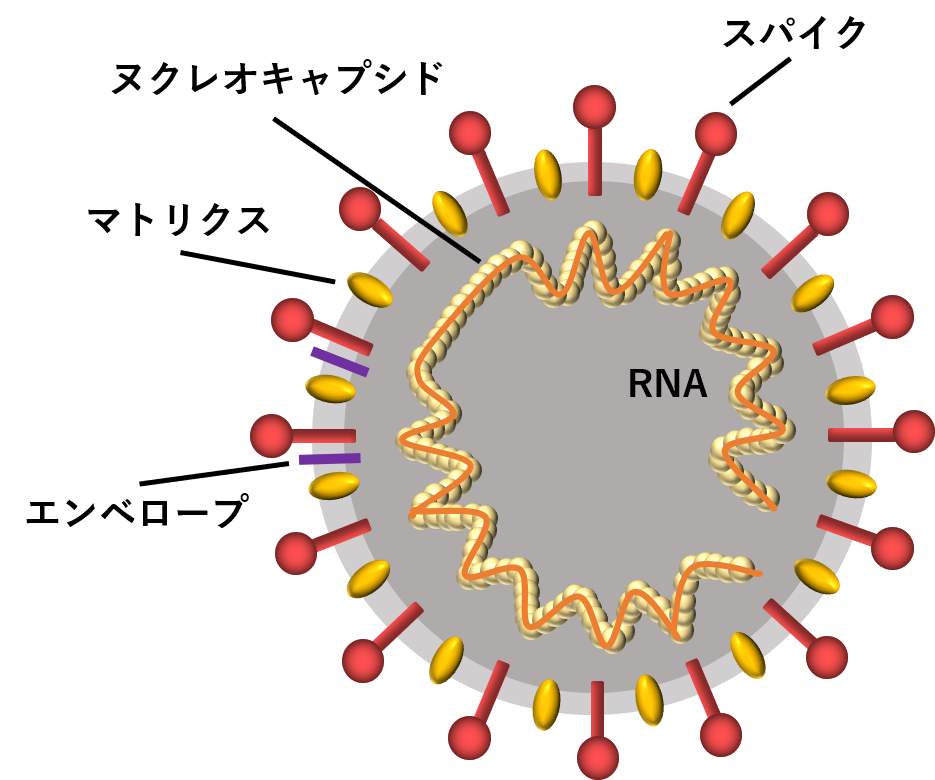
(新型コロナウイルスの模式図。スパイクと呼ばれているタンパク質を測定しています。それによってウイルスの検出特異性を確かなものにしました。)
(3)そのために新しく開発した手法
新型コロナウイルスのスパイクタンパク質を特異的に認識する抗体を2種類用意し、その2種類の抗体で新型コロナウイルスのスパイクタンパク質をサンドイッチ方式で挟み込みました。1種類の抗体にはアルカリホスファターゼという酵素を標識しておき、そこにリン酸基がついた基質を作用させます。アルカリホスファターゼの働きによって、その基質からリン酸基が外れます。次に、その基質をチオNADサイクリング法で増幅します。サイクリングでは水酸化ステロイド脱水素酵素が中心の酵素となり、それ以外にNADHやチオNADを加えておくことで、サイクリング中にチオNADHが溜まっていきます。このチオNADHの吸光度変化(405 nm)を測定することで、元の新型コロナウイルスのスパイクタンパク質が測定できます。吸光度変化を測定するだけなので、特別な機器は不要となりマイクロプレートリーダーで検査でき、試薬類もPCRに比べてはるかに安価です。将来的には約30分程度でウイルス検出できることを目指しています。
(4)研究の波及効果や社会的影響
PCR検査は感度が良いものの、検出結果が出るまで2日程度の時間を要すること、技術的な問題で偽陰性が出やすいこと、活性を持たない(=死んだ)ウイルスも検出してしまい陽性判定となる場合があること、どこのクリニックでも実施できるわけでは無いので中核病院や保健所の臨床検査技師への負担が大きいこと、などの問題が山積みです。新たな検査法を用いれば、吸光度を測定するだけで、町医者などの一般クリニックでも検査が可能になります。すなわち、新型コロナウイルス感染症に対する、迅速・簡単・安価・高特異性・高感度の「抗原検査法」として利用可能です。
(5)今後の課題
早稲田大学にはバイオセーフティーレベル3の実験室がありません。設置が大変難しく、これは多くの大学・企業にとって普通のことです。そこで、今後、公的研究機関などの協力を得て、実際の患者検体での測定を早急に試す必要があります。
(6)用語解説/出典情報
※1 ELISA法
今回はサンドイッチ法を用いて、特異性の高い2種類の抗体で標的タンパク質を挟みこんで検出しています。2次抗体側にはアルカリホスファターゼが標識されています。
※2 酵素サイクリング法
酵素の働きによって、基質をサイクリングさせることで増幅させ、極微量の物質の濃度を測定するための方法。本来、酵素サイクリング法は時間に対してシグナルは線形応答しますが、ELISA法と組み合わせることでシグナルが三角数として増加します。さらに当研究グループでは、サイクリングの正反応・逆反応のために1種類の酵素だけを利用し、ノイズを低減させています。
※3 アットモル
10-18モル、個数でいうと100万個に相当します。通常のELISA法では高感度として市販されているものでも10-15モル程度なので、1000倍以上の高感度化に成功しています。
※4 化学発光酵素免疫測定法
我々の方法はサンドイッチELISA法を用いており、2種類の抗体で標的タンパク質を挟みこんでいます。この化学発光酵素免疫測定法もその点は一緒です。ただし、我々の方法では、ELISA法のあとで、そこで得られるシグナルを酵素サイクリング法で増幅することによって、結果として、極微量の標的タンパク質を検出しています。一方で、この化学発光酵素免疫測定法ではそのような増幅をすることなく、反応させる基質に化学発光基質を用いて、その発光強度を測定しているわけです。ある意味、手間を掛けない分だけ、一見良いようにも見えますが、実は、発光反応を測定することが必須であるため、発光光度計などの特殊専門装置が必要となります。すなわち、どこでも測定できるわけでもなく、診断価格も高くなります。我々の方は、逆に手間を掛けていますが、単純な比色反応で済みますので、どこでも測定でき、診断価格も安価に抑えられます。
出典1:『Coronavirus antigen tests: quick and cheap, but too often wrong?』
出典2:『Advice on the use of point-of-care immunodiagnostic tests for COVID-19』
(7)論文情報
雑誌名:Diagnostics
執筆者名(所属機関名):Yuta Kyosei(早稲田大学)、Mayuri Namba(早稲田大学)、Sou Yamura(早稲田大学)、Rikiya Takeuchi((株)タウンズ)、Noriko Aoki((株)タウンズ)、Kazunari Nakaishi((株)タウンズ)、Satoshi Watabe((株)タウンズ)、Etsuro Ito(早稲田大学)
DOI:10.3390/diagnostics10080594
(8)研究助成
研究費名:科学技術振興機構(JST) 研究成果最適展開支援プログラム(A-STEP)
研究課題名:高病原性鳥インフルエンザウイルスの迅速高感度検出システムの開発(JPMJTR184B)
研究代表者名(所属機関名):研究責任者 伊藤悦朗(早稲田大学)、プロジェクトリーダー(企業責任者) 太田俊也(株式会社タウンズ)







