ゲノムDNAの構造をこわれやすくして遺伝子の転写を制御するしくみを解明
1. 概要
ゲノム中の遺伝子がタイミングよく使われる、つまり“転写”されることは、全ての生命活動に重要です。しかし真核生物のゲノムDNA は、細胞核内で折りたたまれています。その折りたたみ構造では、タンパク質の複合体であるヒストン8量体にDNAが巻きつき、“ヌクレオソーム”と呼ばれるコンパクトな構造をとっております。そのため、そのままでは転写がされにくい状態になっています。タンパク質にならないリボ核酸(“ノンコーディングRNA”と呼ばれる)は、転写を調節することがあると提唱されていますが、ヌクレオソームにどのような影響を持つかはわかっていませんでした。
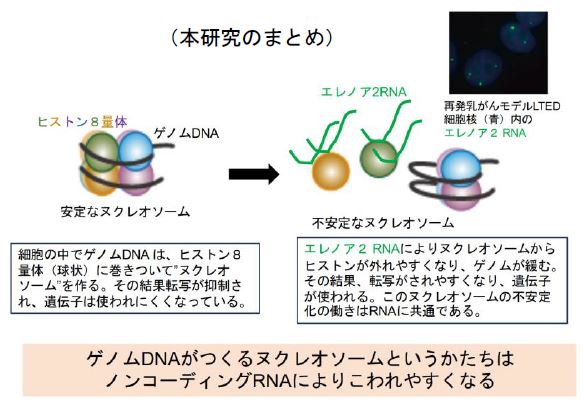
- 早稲田大学理工学術院浜田道昭教授、東京大学定量生命科学研究所の胡桃坂仁志教授、公益財団法人がん研究会がん研究所斉藤典子部長らの研究グループは、熊本大学との共同研究により、核内のノンコーディングRNA にはヌクレオソームをこわれやすくして転写をコントロールする、という新しいはたらきがあることを発見しました。
- エレノア2ノンコーディングRNAは、再発乳がんモデル細胞で、エストロゲン受容体遺伝子座の周辺からつくられ、そこに蓄積して転写を活発にさせます。この再発乳がん細胞では、エレノア2がつくられる周辺でヌクレオソームが緩んでおり、エレノア2を減弱するとこれが解消されました。
- 試験管内の実験では、人工的に作成したエレノア2 RNA 断片が、ヌクレオソームを著しく不安定化することを明らかにしました。このヌクレオソームを不安定化する、という活性は他のRNA にも認めらましたが、DNAにはありませんでした。
- 本研究の成果は、Nature Publishing Groupオープンアクセス誌Communications Biologyに、2020年2月11日付で公開されました。
2. ポイント
- 再発乳がんモデル細胞(注1)では、ゲノムからエレノア2ノンコーディングRNA(注2)が過剰に転写(注3)されつくられますが、その近くではゲノムが作る高次構造であるヌクレオソーム(注4)が緩んでいました
- 人工的な試験管の中の実験でも、エレノア2 RNA 断片がヌクレオソームを著しく不安定にしました。
- 核内のノンコーディングRNA には、ヌクレオソーム構造を緩めて転写を制御するという新しい機能があることを発見しました。
3. 論文名、著者およびその所属
○論文名: Nucleosome destabilization by nuclear non-coding RNAs.
○ジャーナル名: Communications Biology (Nature Publishing Groupのオープンアクセス誌)
(※2020年2月11日付でオンラインに掲載されました。doi: 10.1038/s42003-020-0784-9)
○著者: Risa Fujita1#, Tatsuro Yamamoto2,3#, Yasuhiro Arimura1, Saori Fujiwara3+, Hiroaki Tachiwana2, Yuichi Ichikawa2, Yuka Sakata2, Liying Yang2, Reo Maruyama2, Michiaki Hamada4,5, Mitsuyoshi Nakao3, Noriko Saitoh2*, and Hitoshi Kurumizaka1*
# 共同第一著者 * 責任著者
○著者の所属機関
1. 東京大学定量生命科学研究所
2. 公益財団法人がん研究会がん研究所
3. 国立大学法人熊本大学発生医学研究所
3+. 国立大学法人熊本大学発生医学研究所(研究当時)
4. 早稲田大学大学院先進理工学研究科
5. 産総研・早大生体システムビッグデータ解析オープンイノベーションラボラトリ
4. 研究の詳細
背景と経緯
ゲノムDNAは細胞核の中で、クロマチンとよばれるコンパクトな形となって納められています。クロマチンの基本構造はヌクレオソームとよばれるもので、およそ150 塩基対のDNA が2つのヒストンH2A-H2Bと2つのH3-H4からなるヒストン8量体に巻きついたものです。ヌクレオソームは非常に安定で、転写を含むゲノムDNAの機能を抑制するものです。
ノンコーディングRNAはタンパク質にならないRNAで、生体内で多種多様に存在し、ゲノム機能を制御します。
ESR1はエストロゲン受容体(ER)タンパク質をコードする遺伝子で、ER陽性乳がんが、内分泌療法を模したホルモンを枯渇した状況(long-term estrogen deprivation を略してLTEDと呼ばれる)に適応する際にさかんに転写されます。その際にエレノアとよばれる一群のノンコーディングRNAが、たくさんつくられます。LTED細胞核の中で、エレノアは自身が転写されるゲノム部位にたまり、その結果、ESR1遺伝子の転写を活性化します。エレノア同様に、細胞核内に蓄積するようなノンコーディングRNAは多々あります。しかし、エレノアを含め核内のノンコーディングRNAがどのように転写を活性化するかについて、そのしくみは不明でした。
研究内容
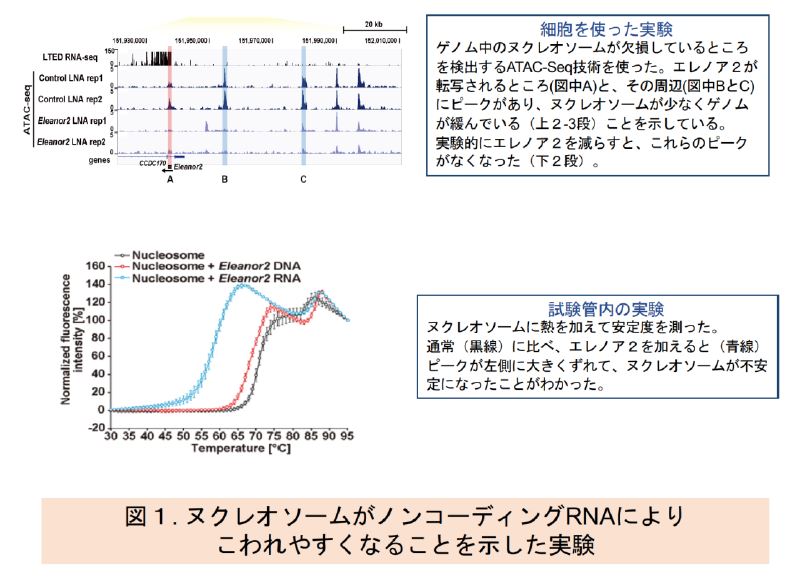
本研究者らはまず、ゲノム中のクロマチンが緩んでいる箇所を検出する技術である、FAIRE-Seq (formaldehyde-assisted isolation of regulatory elements, coupled with massively parallel sequencing) の過去のデータを解析しました(図1上)。その結果、LTED細胞ではESR1遺伝子の上流域でヌクレオソームが著しく欠損していることを見いだしました。この付近では、エレノアの中でも最も多いエレノア2がさかんにつくられていました。
そこで精細な試験管内実験を行ったところ、エレノア2のRNA断片が、ヌクレオソーム内のH2A-H2Bを不安定化することによって、ヌクレオソームを不安定にすることを発見しました(図1下)。このヌクレオソーム不安定化活性は、他のノンコーディングRNAであるMALAT1、DSCAM-AS1、XISTにも検出されましたが、一定の構造をとらないpoly(U) RNA やDNAにはありませんでした。
さらにLTED細胞内でエレノア2の量を減少させて、ヌクレオソームの欠損を検出するATAC-Seq (Assay for Transposase-Accessible Chromatin using sequencing)という解析を行いました。その結果、エレノア2の転写部位ではピークが小さくなっており、これはヌクレオソームが安定にもどっていることを示すものでした(図1上)。
まとめ
本研究では、エレノア2ノンコーディングRNAが、試験管内と細胞内のどちらにおいても、ヌクレオソームを不安定にすることを明らかにしました。これは、エレノア2が再発乳がんでESR1遺伝子を使われやすくしているしくみと考えられます。なお、ヌクレオソームをこわす活性は他の様々なRNAにもあることもわかり、RNAが共通してもつ固有の性質といえそうです。
5. 本研究への支援
本研究は、下記機関より資金的支援等を受けて実施されました。
- 文部科学省科学研究費補助金・新学術領域研究「遺伝子制御の基盤となるクロマチンポテンシャル」
- 日本学術振興会科学研究費補助金基盤研究、挑戦的研究、若手研究
- JST (科学技術振興機構) CREST
- AMED (革新的先端研究開発支援事業) CREST
- JST (科学技術振興機構) ERATO
- 武田報彰医学研究助成
- 三菱財団自然科学研究助成
6. 用語解説
(注1)再発乳がんモデル細胞
- ヒトER陽性乳がん細胞株MCF7を、3ヶ月以上の長期にわたってエストロゲンを枯渇した状態で培養して、生き残る細胞。LTED(long-term estrogen deprivation)細胞とよばれる。もとのMCF7 細胞とは異なり、エストロゲンがなくても増えることができる。
(注2)ノンコーディングRNA
- タンパク質に翻訳されない種類のRNA(リボ核酸)。細胞質でリボソームによりタンパク質になるメッセンジャーRNAとは異なり、細胞や生命の制御因子と推定される。ヒトには10万種類ほどのノンコーディングRNAが存在すると見積もられており、多くが細胞核内に存在する。いくつかのノンコーディングRNAについては、がんを含む疾患に関わることがわかってきている。
(注3)転写
- 遺伝情報の本体であるDNA(デオキシリボ核酸)の塩基配列が、RNA合成酵素によってコピーされて、RNAが合成されること。一般的に遺伝子の機能は、DNAが転写されてRNAになり、それがタンパク質に翻訳されることによって発現する。
(注4)ヌクレオソーム
- 真核生物のゲノムDNAが細胞核内でとるクロマチンの基本構造単位。4種類のヒストンタンパク質(H2A、H2B、H3、H4)が2分子ずつから構成されるヒストン8量体の周囲にDNA二重らせんが約1.5回ほど、巻きついたもの。







