ナノチューブ膜スタンプで細胞内液・ミトコンドリアを直接移送
~細胞機能を最大25%向上させる新しい「細胞手術」技術を開発~
発表のポイント
- 細胞内液やミトコンドリアを別の細胞へ直接移送できるスタンプシステムを開発しました。
- 細胞生存率約95%、物質移送効率約90%という高い性能を実現しました。
- ミトコンドリア移送により、細胞内ATP産生量が最大25%向上することを実証しました。
早稲田大学大学院情報生産システム研究科の三宅 丈雄(みやけ たけお)教授らの研究グループは、ナノチューブ膜を用いたナノ注射器(ナノチューブ膜スタンプ)に圧力制御機構を搭載させることで、細胞内液やミトコンドリアなどの細胞内成分を別の細胞へ高効率かつ高生存率を保ったまま直接移送することに成功しました。
本技術により、従来は困難であった細胞内部成分の抽出・保存・再導入を一体的に制御できるようになり、移送されたミトコンドリアが受容細胞内で機能し、アデノシン三リン酸(ATP)産生を有意に向上させることを世界で初めて定量的に示しました。本成果は、細胞治療、再生医療、細胞機能解析などの分野において、新たな「細胞手術」技術としての応用が期待されます。
以上は、科学研究費補助金、科学技術振興機構(JST) 戦略的創造研究推進事業 さきがけ「電子・イオン制御型バイオイオントロニクス」(JPMJPR20B8)による成果であり、2026年3月17日(火)に科学誌「Small Science」にオンライン版で公開されました。
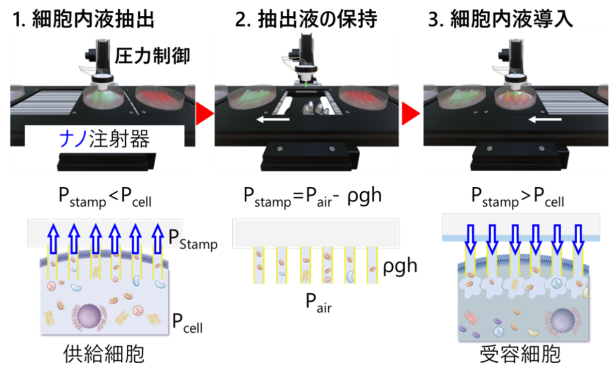
図:圧力制御可能なナノ注射器による細胞内液・ミトコンドリア移送技術
(1)研究の背景
細胞間でタンパク質やRNA、さらにはミトコンドリアなどの細胞内成分が移動する現象は、細胞機能の制御や疾患進展に深く関与していることが知られています。実際、自然界においてはトンネリングナノチューブ(TNT)と呼ばれる細胞間チャネルを介して、ミトコンドリアを含む細胞内成分が細胞間で輸送される現象が報告されており、エネルギー代謝の補償や細胞生存、疾患進行との関連が注目されています。しかしながら、このようなTNTを介した細胞間輸送は、発生頻度が低く、特定の細胞種や病理条件に強く依存することが知られています。また、輸送される分子種やオルガネラ※1、輸送量、方向性を人為的に制御することは未だ実現されておらず、自然界の機能を直接的に医療応用する段階には至っていません。
一方、人工的な細胞操作技術としては、ウイルスベクター、電気穿孔法(エレクトロポレーション)、脂質ナノキャリア(リポフェクション)など、主として「細胞内への導入」に特化した手法が広く用いられてきましたが、これらはいずれも生細胞から細胞内成分を抽出し、別の生細胞へ移送するという双方向操作には対応できません。マイクロインジェクションや原理間力顕微鏡(AFM)などのナノピペットを用いた単一細胞レベルでの吸引・注入操作も報告されているものの、極めて低スループット※2であり、細胞損傷や操作再現性の点から、多数の細胞を対象とした細胞間移送技術としての汎用化には大きな課題が残されています。特に、ミトコンドリアのような機能性オルガネラを細胞機能を維持したまま、意図した細胞間で、かつ多数の細胞へ移送する技術は現在まで確立されておらず、細胞治療や細胞機能再設計を実現する上での技術的ボトルネックとなっています(表1)。

表1:従来技術と本研究技術の比較
(2)研究の成果
本研究では、自然界における偶発的な細胞間輸送(TNT)や、導入のみに特化した既存技術の限界を踏まえ、生細胞から細胞内成分を穏やかに抽出し、別の生細胞へ高効率に導入することを同一プラットフォームで実現するナノ注射器システムを開発しました。本技術は、ナノチューブ内部の圧力を精密に制御することで、抽出・保持・導入という一連の操作を連続的かつ再現性高く行える点に特徴があります。
【要素技術:圧力制御による抽出・保持・導入の一体化】
本研究で用いたナノチューブ注射器は、金ナノチューブ膜とガラス管から構成され、ナノチューブを細胞膜に挿入した状態でガラス管内部の圧力を制御することで、細胞内成分の出入りを制御します。ガラス管内の圧力(Pstamp)が細胞内圧(Pcell)より低い場合には、細胞内液が受動的にナノチューブ内へ流入し、細胞内成分の抽出が行われます。一方で、ガラス管内に緩衝液を加えることで内部圧力を調整すると、過剰な抽出を抑制し、細胞機能を維持したまま穏やかな物質交換が可能となります。本研究では、ナノチューブ内径が大きく、かつ、ナノチューブ密度が多いほど、抽出量は大きくなり、一方、ガラス管に加える緩衝液の量を増やすほど、抽出量は少なくなることがわかりました。特に約200μLの緩衝液をガラス管に入れると、抽出はほぼ抑制されることがわかりました。
一方、抽出された細胞内成分は、ガラス管内を密閉することでナノチューブ内部に一時的に保持されます。その後、導入工程ではガラス管内に緩衝液を追加して正の圧力を与えることで、保持された細胞内成分を標的細胞内へと能動的に押し出すことができます。図1下図に示したのは、チューブ内部に異なる体積のカルセイン液※3を注入した際、どれだけのカルセインが膜を通過したかを示しています。そこでは、ガラス管を細胞が接着している高さまで水に沈めており、その際、200μLと300μLの間でカルセイン通過量に変化があることがわかります。これは、200μL以下では、カルセイン溶液の量が十分でないため、水圧の影響でカルセインの膜通過が減少するのに対し、300μL以上では、水の流れを発生させることができるため、カルセインが十分に通過したと考えています。この圧力制御に基づく操作により、従来は別個の操作として扱われてきた「抽出」と「導入」を一体化し、生細胞を維持したまま双方向の細胞間移送を実現しました(図1下図)。
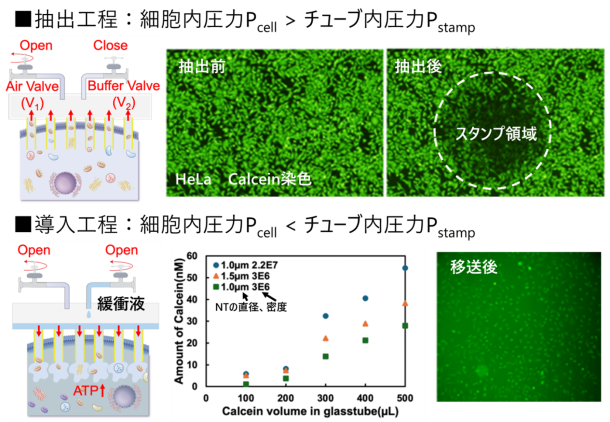
図1:細胞内液抽出および導入結果
【HeLa および NIH-3T3 細胞を用いた同種・異種間移送】
本技術の汎用性を検証するため、HeLa 細胞※4および NIH-3T3 ※5を用い、同種間(HeLa→HeLa、NIH-3T3→NIH-3T3)および異種間(HeLa→NIH-3T3、NIH-3T3→HeLa)での細胞内成分移送を行いました。その結果、いずれの組み合わせにおいても高い移送効率(約90%以上)と高い細胞生存率(約95%以上)が維持されることを確認しました。
特に異種間移送では、外来由来の細胞内成分に起因すると考えられる一時的な増殖抑制が観察されたものの、培養を継続することで細胞は回復し、最終的には正常な増殖挙動を示しました。これは、本技術が細胞機能を致命的に損なうことなく、細胞間で細胞内成分を移送できることを示しています。
【ミトコンドリア移送による細胞機能の向上(図2)】
さらに本研究では、ナノチューブ径の違いがミトコンドリア移送および細胞機能に与える影響を検証しました。ナノチューブ径が0.6μm(内径は約310nm)の場合、ミトコンドリアのサイズに対してチューブ径が小さいため、ミトコンドリアの抽出および移送はほとんど起こらず、標的細胞におけるATP産生量の有意な変化は認められませんでした。
一方、ナノチューブ径を1.5μm(内径は約1260nm)とした場合には、ミトコンドリアを効率的に抽出・移送することが可能となり、標的細胞内にミトコンドリアが実際に取り込まれていることが確認されました。その結果、ミトコンドリアを移送した細胞では、移送後24時間以内にATP産生量が有意に増加し、細胞機能が明確に向上しました。
この結果は、単なる細胞内液の移送では細胞機能の改善は起こらず、機能性オルガネラであるミトコンドリアそのものを移送できた場合にのみ、細胞機能の向上が実現されることを示しています。
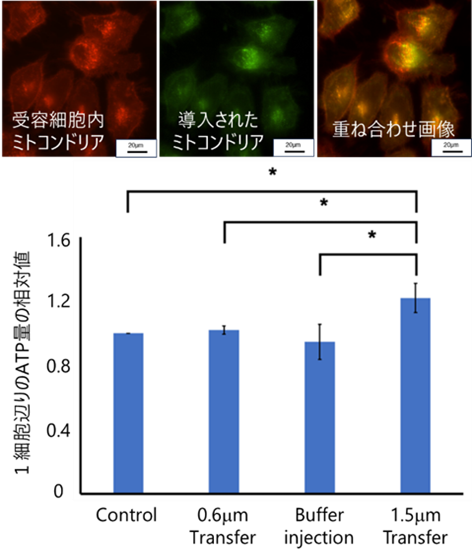
図2:ミトコンドリア移送による機能活性
(3)研究の波及効果や社会的影響
本研究成果は、細胞内成分移送を偶発的現象や特殊操作としてではなく、再現性・定量性を備えた操作技術として確立した点に社会的意義があります。抽出・保持・導入を同一プラットフォームで制御できる本技術は、さらなる自動化・制御機構を搭載することで、細胞操作の信頼性や評価基準の共有を可能とし、細胞を扱う研究・開発分野における操作技術の標準化と品質向上に資する基盤的成果ではないかと考えています。
(4)今後の展望
本研究で開発したナノ注射器は、生細胞から細胞内成分を抽出し、別の生細胞へ高効率に移送できることを実証した基盤技術です。今後は本技術の適用範囲を拡張し、さまざまな細胞種に対する再現性や安定性の検証を進めていく予定です。特に移植可能な細胞を用いた再生医療研究に取り組みたいと考えています。
一方、基礎研究として動物性細胞以外の細胞(植物、酵母、乳酸菌など)にも展開していきたいと考えています。これらを一研究室で実現することは困難ですので、本プロジェクトにご興味のある企業や研究機関との連携を模索していきたいと考えています。
(5)用語解説
※1 オルガネラ:
細胞内部に存在し、特定の機能を担う構造体の総称である。代表的なオルガネラには、エネルギー産生を担うミトコンドリア、タンパク質合成に関与する小胞体、物質の修飾・輸送を行うゴルジ体などがあり、細胞の機能や状態を支える重要な役割を果たしている。
※2 低スループット:
一定時間内に処理・解析できる試料数や対象数が少ないことを指す。細胞操作技術においては、1回の操作で扱える細胞数が限られている、あるいは操作に時間や熟練を要するため、多数の細胞を効率的に処理できない状態を意味する。
※3 カルセイン液:
蛍光色素であるカルセインを溶解した水溶液であり、物質の移動や透過性を可視化・定量評価するための試薬として広く用いられている。カルセインは水溶性が高く、細胞毒性が低いため、膜透過や流体移動の評価に適しており、本研究ではナノチューブ膜を介した物質通過量や圧力制御による移送挙動を評価する指標として用いられた。
※4 HeLa細胞:
世界で最も広く利用されているヒト由来の培養細胞株である。高い増殖能と安定した性質を有し、細胞生物学、がん研究、薬剤評価、細胞操作技術の検証など、基礎から応用まで幅広い研究分野で標準的なモデル細胞として用いられている。
※5 NIH-3T3細胞:
マウス胚由来の線維芽細胞から樹立された培養細胞株で、増殖性が安定しており、細胞増殖、分化、シグナル伝達、細胞操作技術の評価などに広く用いられている標準的なモデル細胞である。
(6)論文情報
雑誌名:Small Science
論文名:A Nanotube Injector for Cytoplasmic Transfer and Enhanced Mitochondrial Function
執筆者名:Bingfu Liu, Zhuhang Dai, Bowen Zhang, Kazuhiro Oyama, Chenxi Li, Yukun Chen,
Mingyin Cui, Takeo Miyake *責任著者
掲載日:2026年3月17日(火)
DOI:10.1002/smsc.202500598
掲載URL:https://onlinelibrary.wiley.com/doi/10.1002/smsc.202500598
(7)研究助成
科学技術振興機構(JST)
戦略的創造研究推進事業 さきがけ「電子・イオン制御型バイオイオントロニクス」(JPMJPR20B8)









