激しい長時間の運動後に生じるお腹へのダメージ
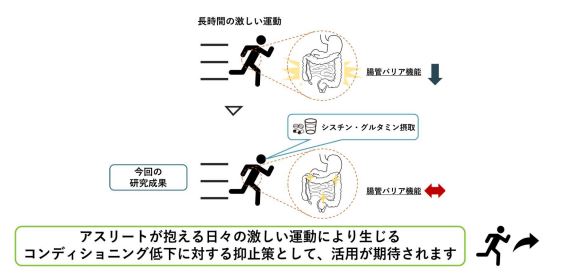
アミノ酸のシスチン・グルタミン摂取により、激しい長時間の運動後に生じる腸管バリア機能の低下を抑制することを確認
発表のポイント
激しい長時間の運動により生じる腸管バリア機能の低下の抑止策として、これまで汎用性の高い研究デザイン(使用する食品・サプリメントの種類や摂取量)で検討されていなかった。
アミノ酸であるシスチン・グルタミン摂取により、激しい運動に伴う腸管バリア機能の低下を抑えることを確認した。
アスリートが抱える日々の激しい運動の反復により生じるコンディショニング低下に対する抑止策として、活用が期待される。
早稲田大学スポーツ科学学術院の宮下政司(みやしたまさし)教授、同大学大学院スポーツ科学研究科修士課程2年在籍の田髙悠晟(たたかゆうせい)と味の素株式会社(東京都中央区、取締役 代表執行役社長 西井孝明)らの研究グループは、一過性の激しい運動が腸管透過性*1に及ぼす影響を評価し、アミノ酸のシスチン*2・グルタミン*3を摂取することで運動により腸管が受けるダメージおよび守る働きの低下を抑制することを明らかにしました。
本研究成果は、Springer Nature発行の『European Journal of Nutrition』に2022年2月1日(火)にオンラインで公開されました。
【論文情報】
雑誌名:European Journal of Nutrition
論文名:Effects of oral cystine and glutamine on exercise-induced changes in gastrointestinal permeability and damage markers in young men
(1)これまでの研究で分かっていたこと(科学史的・歴史的な背景など)
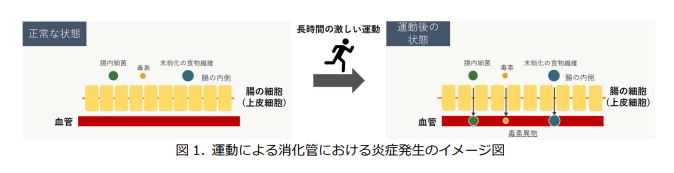
アスリート(特に持久系アスリート)の多くが、運動中および運動後に腹部の不快感を経験していることが報告されています(Oliveira et al. Sports Med. 2014;44(Suppl 1):79–85)。これは、長時間または激しい運動による”体温の上昇”と”消化管機能の低下”によって、細胞に隙間ができ細菌や毒素が腸管内腔から血管内へ漏出しやすくなり、ダメージ(炎症)が生じているために起きている現象である可能性が示唆されています(Costa et al. Aliment Pharmacol Ther. 2017;46(3):246-265)(図1)。このような現象は、アスリートのコンディションあるいはパフォーマンスの低下と関係していることが考えられるため、スポーツ現場における抑止策を確立することは重要です。
このような背景から、これまでの先行研究では、牛の初乳やポリフェノール、ビタミンE、クルクミンなどのサプリメントを用いた腸管バリア機能の低下の抑止策が検討されてきました(Costa et al. Temperature.2020;7(1):58–88)。しかし、これらのサプリメントは、入手が容易ではないことや摂取量が多すぎることが問題点として挙げられます。そのため、多くのアスリートが、日常的に摂取しやすいような、入手が容易かつ低用量のサプリメントの開発や検討が急がれています。
(2)今回の研究で新たに実現しようとしたこと、明らかになったこと
上記で挙げたサプリメント以外に、シスチンの生理作用として腸管の炎症を抑制することが、細胞実験によって報告されています(Hasegawa et al. Amino Acids 2021;53(7):1021–1032)。さらに、グルタミンの生理作用として、激しい運動による腸管バリア機能の低下を抑制することが報告されています(Zuhl et al. J Appl Physiol 2014;116(2):183–191)。しかし、シスチンとグルタミンの組み合わせによるサプリメントとしての摂取が、運動による腸管バリア機能の低下を抑制させるかどうかは、これまで明らかにされていません。
そこで、本研究では、シスチンとグルタミンの組み合わせによるサプリメントの摂取が、長時間の激しい運動による腸管バリア機能の低下に与える影響を検証しました。
(3)そのために新しく開発した手法
健康な若年男性16名(平均年齢23歳)を対象に、サプリメントの摂取を1日3回、計6日間継続してもらいました。サプリメントはプラセボとシスチン・グルタミンの2つを用意し、各サプリメントの摂取期間をそれぞれ、Placebo試行とCys2/Gln試行*4としました。なお、サプリメント摂取1回あたりのシスチンとグルタミンの含有量は、それぞれ、0.23 gと1.0 gとしました。実験デザインは、全対
象者が両試行に参加するクロスオーバー法*5を用いました(図2)。
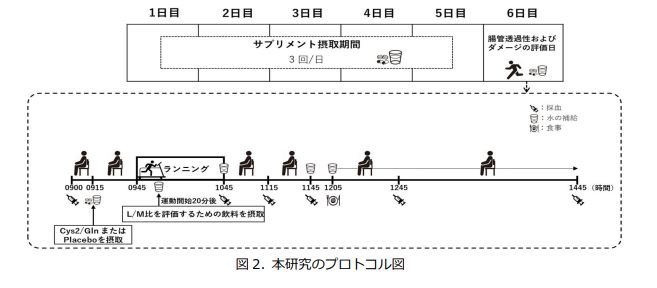
運動は、トレッドミル(ランニングマシン)を用いたランニングとし、最大酸素摂取量の75%に相当する速度で1時間実施し、長時間の激しい運動となるように設定しました。腸管透過性と腸管のダメージの評価には、それぞれラクツロースとマンニトールの比(L/M比)*6と腸管中脂肪酸結合タンパク質(I-FABP)*7の2つの測定項目を用いました。
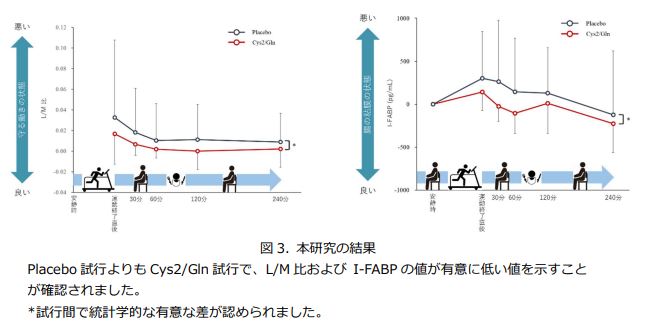
結果は次の通りです。ランニング後のL/M比とI-FABPは、Cys2/Gln試行でPlacebo試行よりも有意に低い値を示しました。この結果は、シスチン・グルタミンのサプリメントを1日3回、計6日間継続して摂取することで、長時間の激しい運動による腸管バリア機能の低下が抑制される可能性があることを意味しています(図3)。
(4)研究の波及効果や社会的影響
激しい長時間の運動による腸管バリア機能の低下は高温・多湿環境下でより顕著に表れます(熱ストレスが、運動による消化管へのダメージをさらに増大させるためです)。しかし、本研究のように高温環境下での運動でなくとも腸管バリア機能の低下を確認し、シスチン・グルタミンの摂取によってその機能低下の抑制を確認しました。本研究結果の現場への汎用性として、低用量のシスチンとグルタミンサプリメントを継続的に摂取することで、アスリート(特に持久系アスリート)の多くが、長時間の激しい運動中と運動後において経験しているとされる腹部の不快感の発生を予防し、ベストなコンディションでパフォーマンスを発揮できるようになることが期待されます。
(5)今後の課題
今後は、慢性的な運動トレーニングに伴い腹部に不快感を抱えるアスリートを対象にシスチン・グルタミンの摂取によって、これらの症状が抑えられるかを調査する必要があります。
(6)研究者のコメント
これまで運動前後の栄養介入として、身体全体への代謝動態(糖・脂質代謝)*8を主軸として研究に取り組んできました。本研究では、激しい運動で生じる疲れを筋肉や代謝動態の変化ではなく、「お腹」に着目し、味の素株式会社との共同研究により、目標を達成することができました。得られた知見を活かし、引き続き、栄養素の質や組み合わせによる研究に取り組みたいと思います。
(7)用語解説
※1 腸管透過性
腸におけるフィルター機能の働きを指します。通常、上皮細胞がきれいに並んで(細胞間の密着結合)バリア(障壁)を形成しますが、激しい長時間の運動を行うことで、細胞に隙間ができ細菌や毒素が腸管内腔から血管内へ漏出します。
※2 シスチン
20種類あるアミノ酸のうち、体の中で作られるアミノ酸の一つであるシステインが二つ合わさったものです。
※3 グルタミン
血液中に最も豊富に含まれ、体の中で作られるアミノ酸です。
※4 Placebo試行とCys2/Gln試行
Placebo試行: 2.46 gのマルトデキストリンを1日3回、摂取する試行です。
Cys2/Gln試行: 0.23 gのL-シスチン、00gのL-グルタミンおよび1.23 gのマルトデキストリンを1日3回、摂取する試行です。
※5 クロスオーバー法
複数の試行が存在する場合、個体要因を排除するために、全対象者が各試行間に休息期間(ウォッシュアウト期間)を設けながら、全ての試行に参加する方法です。
※6 ラクツロースとマンニトールの比(L/M比)
2種類の非消化糖類のラクツロース(Lactulose),マンニトール(Mannitol)を含む試験液を摂取し,その吸収率の比(ラクツロースは透過しにくい糖類で、マンニトールは透過しやすい糖類です)から腸透過性を評価する手法です。腸管透過性の上昇は、腸を守る働きの状態が悪化していることを意味します。
※7 腸管中脂肪酸結合タンパク質(I-FABP)
FABPは小腸粘膜に特異的に分布し、腸管がダメージを受けた際には、血中に放出されます。そのため、血中におけるI-FABPの濃度は、腸の粘膜の状態を意味する指標となります。
※8 代謝動態(糖・脂質代謝)
運動中または運動後のヒトの生体内における主なエネルギー源は、体内のエネルギー状態に合わせて運動強度や運動時間によって、糖質中心または脂質中心に切り替わります。
(8)論文情報
雑誌名:European Journal of Nutrition
論文名:Effects of oral cystine and glutamine on exercise-induced changes in gastrointestinal permeability and damage markers in young men
執筆者名(所属機関名):Yusei Tataka*b, Miki Haramura*c, Yuka Hamada*c, Miho Ono*d, Sakiko Toyoda*e, Toshiyuki Yamada*f, Katsuhiko Suzuki*a, Masashi Miyashita*a
*a Faculty of Sport Sciences, Waseda University
*b Graduate School of Sport Sciences, Waseda University
*c Waseda Institute of Sport Sciences, Waseda University
*d Institute of Food Sciences and Technologies, Ajinomoto Co., Inc.
*e Research Institute for Bioscience Products & Fine Chemicals, Ajinomoto Co., Inc.
*f Sports Nutrition Department, Ajinomoto Co., Inc.
オンライン掲載日:2022年2月1日(火)
掲載URL:https://link.springer.com/article/10.1007/s00394-022-02806-1
DOI:https://doi.org/10.1007/s00394-022-02806-1







