早稲田大学理工学術院の木野邦器(きのくにき)教授、原良太郎(はらりょうたろう)次席研究員(研究院講師)、鈴木伸(すずきしん)助手(先進理工学研究科博士後期課程2年)、先進理工学研究科修士課程2年(当時)の平井健吾(ひらいけんご)氏らの研究グループは、非リボソーム型ペプチド合成酵素の一部分であるアデニル化ドメインを用い、カルボン酸を活性化することで任意のアミンとアミド結合を形成するメカニズムを明らかにしました。本手法を用いることで、アミノ酸どうしの組み合わせに限定しない多様なアミド化合物の触媒的合成が可能となります。
本研究成果は、英国Nature Publishing Groupのオンライン科学雑誌『Scientific Reports』に2018年2月13日に掲載されました。
研究成果の概要
アミド結合形成反応は化学合成における重要な反応のひとつであり、医薬品から汎用化成品の合成に至るまで、重要な工業的反応法として幅広く利用されている。有機合成反応でアミド結合を形成する場合、例えば、カルボン酸とアミンを連結する際には、カルボキシ基を活性化するために縮合剤を用いるのが一般的である。実験室レベルでは効率の良い方法も知られているが、生成物と等モル量の縮合剤や多量の有機溶媒が必要であるなど、工業的利用においては多くの課題がある。近年、触媒的アミド結合形成が注目を集めているが、カルボン酸とアミンを用いた直接的アミド結合形成はボロン酸誘導体を触媒とした報告に限られている。
木野教授はこれまでに、短鎖ペプチド合成研究を中心に、多様な微生物由来アミノ酸リガーゼを利用した触媒的アミド合成法の開発に成功している。当該酵素反応においては、ATP(*1)のエネルギーを利用してアミノ酸をリン酸エステル化し、異なるアミノ酸を求核剤として作用させることでアミド化合物であるペプチドが合成できると考えられている。本研究では、アミノ酸を活性エステル化する異なる種類の酵素であるアデニル化酵素に着目し、当該酵素を利用した触媒的アミド結合形成反応を検討した。その結果、アミノ酸どうしの組み合わせに限定しない多様なアミド化合物の合成法の開発に成功した。
研究成果のポイント
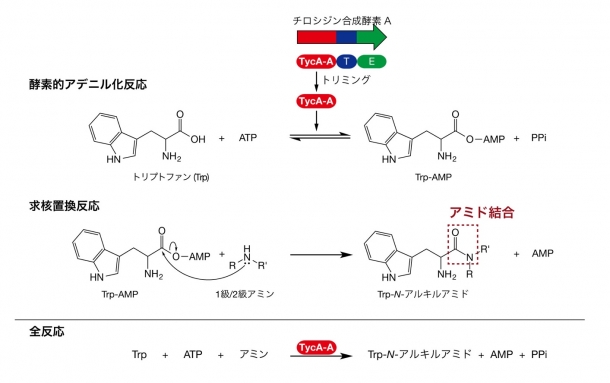
非リボソーム型ペプチド合成酵素(*2)のアデニル化ドメインを用いてアミノ酸をアデニル化し、様々な求核剤(1級/2級アミン)を作用させることにより、アミノ酸の一種であるトリプトファンと、アミン類の間にアミド結合を形成するメカニズムを明らかにした。この発見は、アミノ酸を酵素的に活性化し、任意のアミンを求核剤として利用することによってペプチドの限定しない多様なアミノ酸アミドを触媒的に合成可能であることを示すものである。また、D-アミノ酸も求核剤として利用可能であるため、L-体とD-体の任意の組み合わせによるペプチド合成も可能となり、近年注目されているペプチドの用途開発を大きく広げる可能性を秘めている。
用語説明
- *1 ATP
アデノシン5′-三リン酸。1分子中に高エネルギーリン酸結合を有するヌクレオチドである。エネルギーを要する生体内の反応素過程において、全ての生物に共通して使用され、生体のあらゆる組織に存在するため、エネルギー通貨とも呼ばれる。 - *2 非リボソーム型ペプチド合成酵素
ペプチド抗生物質などの二次代謝産物の生合成に関わる巨大酵素タンパク質であり、複数のモジュールから構成されている。モジュールはさらにドメインと呼ばれる個別の領域にわけられ、アデニル化ドメイン、チオール化ドメイン、縮合ドメインなどが存在する。
論文情報
- 掲載誌:Scientific Reports 8:2950 (2018), DOI: 10.1038/s41598-018-21408-8
- タイトル:A chemoenzymatic process for amide bond formation by an adenylating enzyme-mediated mechanism
- 著者:Ryotaro Hara1, Kengo Hirai2, Shin Suzuki2, Kuniki Kino1,2
1 Research Institute for Science and Engineering, Waseda University, Tokyo, Japan
2 Department of Applied Chemistry, Faculty of Science and Engineering, Waseda University, Tokyo, Japan







