早稲田大学理工学術院 片岡淳(かたおかじゅん)教授らの研究チームは、東京女子医科大学、京都府立医科大学、量子科学技術研究開発機構、名古屋陽子線治療センター、名古屋大学と共同で、陽子線の照射によって体内の原子核で起こるミクロな物理現象を可視化する画期的な手法を確立しました。
医療の進歩によりガン(癌)の根治が期待できるようになった現代では、ただ治すだけでなく治療後には健康な生活を送ることが望まれています。放射線を用いたガン治療は体にメスを入れる必要がないため、患者さんの負担を低減することができます。特に、陽子線と呼ばれる放射線は止まる直前になるとエネルギーを一気に解放する性質を持つため、体の奥深くに位置するガンにもダメージを集中させることができます(※注1)。ガンに対して的確な照射を行えたかどうか逐一確認することが理想的ですが、陽子線がどのように体内を進み、どの組織にどれだけのダメージを与えたかを直接目で視ることはできません。そこで、陽子線が体内を進む過程で原子核に衝突した際に生成される「陽電子放出核種」と呼ばれる特殊な原子核の生成分布をPET装置で捉えることで、陽子線の進路を可視化することが考えられますが、これまで医療に求められる精度でPET計測をシミュレーションすることが困難でした。
今回、本研究チームは陽電子放出核種から生じるチェレンコフ光に着目しました。チェレンコフ光とは、紫外線から可視光領域にまたがる青白い微弱光です。本研究では、その生成頻度を簡単かつ正確に導出する画期的な手法を確立しました。本手法により得られた結果は従来のデータベースを刷新する高い精度を誇り、この結果を用いることで初めて、PET計測を正確にシミュレーションできるようになりました。今回の研究成果は「放射線を視ながらガンを治す」次世代の陽子線治療を実現するうえで重要な役割を担うだけではなく、核物理学や量子力学、素粒子物理学といった基礎物理学の研究で標準的に用いられるデータベースの大幅な精度向上に貢献することが期待されます。
本研究成果は英国Nature Publish Groupのオンライン科学誌『Scientific Reports』に2月7日に掲載されました。
研究の背景
医療の進歩によりガン(癌)の根治が期待できるようになった現代では、ただ治すだけでなく治療後には健康な生活を送ることが望まれています。放射線を用いたガン治療は体にメスを入れる必要がないため、患者さんの負担を低減することができます。特に、陽子線と呼ばれる放射線は止まる直前になるとエネルギーを一気に解放する性質を持つため、体の奥深くに位置するガンにもダメージを集中させることができます(※注1)。ガンに対して的確な照射を行えたかどうか逐一確認することが理想的ですが、陽子線がどのように体内を進み、どの組織にどれだけのダメージを与えたかを直接目で視ることはできません。
人体に照射した陽子線が体内を進む過程で原子核に衝突すると、その衝撃によって陽電子放出核種と呼ばれる特殊な原子核が生成します。陽電子放出核種の近傍からは180度反対の方向に進む2本の対消滅ガンマ線が発生するため、それらをPET装置で捉えれば陽電子放出核種の生成分布を可視化できます。
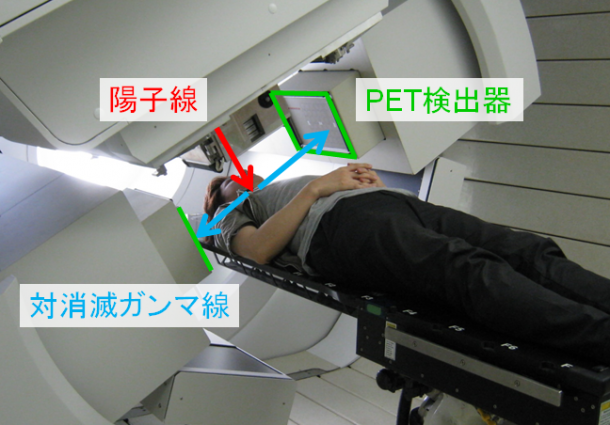
図1 国立がん研究センター東病院の陽子線・PET装置(※注2)
予め「陽電子放出核種の生成頻度」を正確に把握し、各組織に陽子線が与えたダメージをPET画像から見積もることができます。しかしながら、陽電子放出核種はミクロな世界で起こる複雑な現象の副産物であるため、正確な生成頻度は知られておりません。従来のデータを基にシミュレーションを行っても、PET測定を医療に求められる精度で模擬することはできませんでした。そこで、本研究では陽電子放出核種から生じるチェレンコフ光に着目し、その生成頻度を簡単かつ正確に導出する画期的な手法を確立しました。
開発した手法
陽子線と原子核の衝突は核反応と呼ばれる物理現象であり、その反応頻度は核反応断面積と呼ばれる物理量で表されます。核反応によって生成した陽電子放出核種は半減期(※注3)に従って陽電子を放出します。放出された陽電子の中には物質中で光速を超えるものもあり、光速を超えた陽電子はチェレンコフ光と呼ばれる紫外線から可視光領域にまたがる青白い微弱光を放出しながら進みます。陽電子は最終的に2本の対消滅ガンマ線を180度反対の方向に放出します。
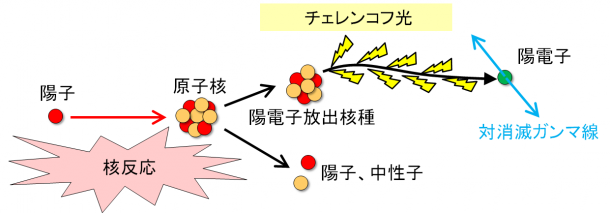
図2 陽電子放出核種の生成機構と反応の模式図
PET装置は2本の対消滅ガンマ線を同時に計測することで陽電子放出核種の画像化を行いますが、本研究では核反応の発生頻度をより詳細に調べるため、陽電子の飛跡に沿って生じるチェレンコフ光に着目しました。CCDカメラを用いることでPET画像の数十倍も高い空間分解能と感度を達成することができました。
結果
人体は水素、酸素、炭素、カルシウムなど数多くの元素から成りますが、陽子線との核反応では酸素が最も重要な原子核となります。そこで本研究では陽子と酸素原子核の核反応断面積を調べることに焦点を当て、酸素を豊富に含み透明な物質である石英ガラス(SiO2)を選定しました。量子科学技術研究開発機構 放射線医学総合研究所のAVF-930サイクロトロンを用いて陽子線の石英ガラスへの照射実験を行いました。
図3は陽子線照射後に石英ガラス中で発生したチェレンコフ光をCCDカメラによって撮像したものです。時間の経過とともに分布が変化しているのは半減期が異なる複数種類の陽電子放出核種が寄与しているためです。この時間発展を詳細に追うことで酸素原子核16Oから3種類の陽電子放出核種15O、13N、11C(半減期は順に122秒、598秒、1222秒)が生成したことを解明し、その分布を切り分けることに成功しました。
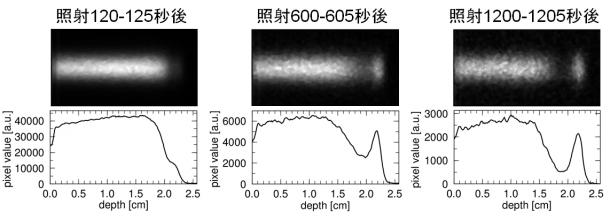
図3 測定したチェレンコフ光とその1次元分布の時間発展
陽子線はエネルギーを失いながら石英ガラス中を進むため、その深度分布はエネルギー分布として捉えることができます。実験データから導出した核反応断面積を図4に示します。図4には比較として米国立核データセンター(NNDC)に収録されている過去の測定値と、INCLと呼ばれる最新の原子核コードを用いたモデル計算の結果が載せてあります。本手法では一度の測定で非常に多くのデータを取得することが可能であり、過去の測定値に比べてばらつきや誤差が小さいことがわかります。また、原子核モデルを用いた計算結果は実験で得られる値から大きく外れてしまうことが分かります。
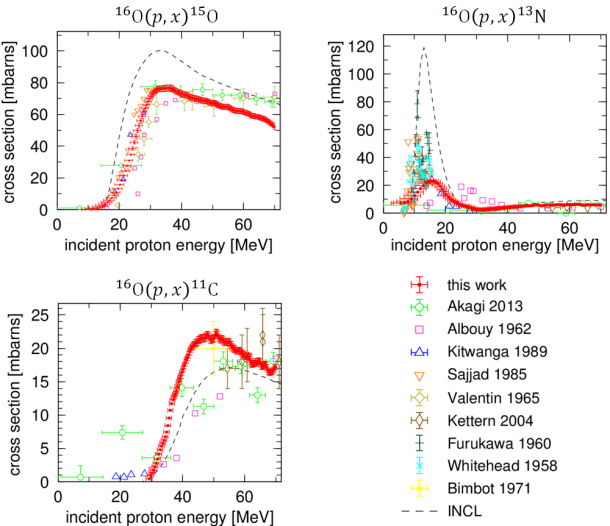
図4 本研究で得られた陽電子放出核種の生成核反応断面積
シミュレーション精度の向上
過去の測定結果には実験毎に大きなばらつきがあり、モデルから得られる計算結果は実験値と明らかに異なることが分かりました。そのため、既存のデータと比べるだけでは本手法の妥当性を証明できません。そこで我々はチェレンコフ光の発生分布より導出した核反応断面積をシミュレーションに組み込み、陽子線照射後にPET装置で得られる陽電子放出核種の分布を再現しました。図5の上段に最新の原子核コードであるINCLを用いた場合の結果を、下段に本手法により得られた核反応断面積を用いた場合の結果をそれぞれ示します。黒いマーカーのPET測定値と赤い実線のシミュレーション結果が一致すれば正しい断面積を使用していると言えます。最新の原子核コードを用いてもPETの測定データを再現することはできませんが、本研究結果を用いることで正しく再現できるようになりました。
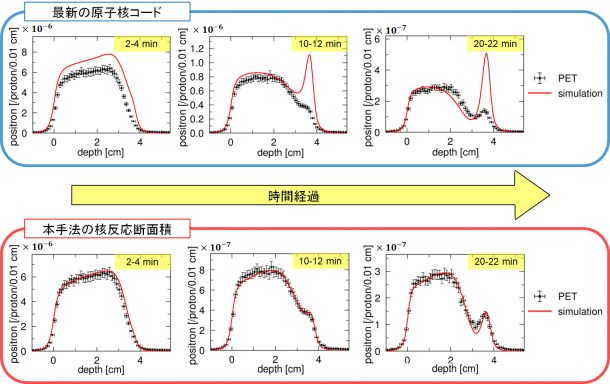
図5 (上) 原子核コードINCLを用いたシミュレーションとPET測定の比較
(下) 本手法により得られた核反応断面積を用いたシミュレーションとPET測定の比較
本研究の成果
本研究では陽子線照射によって陽電子放出核種が生成する核反応の断面積取得法を新たに確立しました。測定したいターゲットに陽子線を照射し、側方に置いたCCDカメラで光を捉えるという非常にシンプルな実験系でありながら、今までに前例の無い精度で物理量を得ることに成功しました。この結果を用いることで、陽子線照射中に体内で生じるミクロな物理現象を正確に再現できるようになりました。今後、本研究成果を米国立核データセンター(NNDC)のライブラリに登録するための手続きを行う予定です。
本研究で得られた成果はPET装置の持つポテンシャルを最大限に引き出す鍵となっており、「放射線を視ながらガンを治す」次世代の陽子線治療を実現する上で重要な役割を担います。それだけではなく、本手法を用いることで核物理学や量子力学、素粒子物理学といった基礎物理学の研究で標準的に用いられるデータベースの大幅な精度向上も期待できます。
今後の課題
今後は本研究で確立した手法を用いて、陽子線治療中に生じる様々な核反応のデータを網羅的に取得する予定です。ただし、陽電子放出核種の生成分布から体内での陽子線の挙動を正確に知るためには、物理学的な現象だけでなく生体内での生物学的な応答も把握する必要があります。また、放射線治療の世界では線量と呼ばれる指標を基に議論するため(※注1)、PET装置で得た陽電子放出核種の生成分布から体内での陽子線の線量分布に変換するようなアルゴリズムを考案する必要もあります。高精度な陽子線治療を達成するためには、医学を中心に物理、化学、生物、数学、情報といった理工学の英知を結集し、問題解決に取り組むことが重要です。
論文情報
・掲載誌:Scientific Reports
研究メンバー
- 早稲田大学大学院 先進理工学研究科 物理学及応用物理学専攻 片岡研究室
増田孝充(実験リーダー)、片岡淳、有元誠、髙部美帆
- 東京女子医科大学大学院 医学研究科 内科系専攻 医学物理学分野
西尾禎治
- 京都府立医科大学 放射線診断治療学講座
松下慶一郎
- 量子科学技術研究開発機構 放射線医学総合研究所 加速器工学部
稲庭拓
- 名古屋市立西部医療センター 名古屋陽子線治療センター
歳藤利行
- 名古屋大学大学院 医学研究科 医療技術学専攻 医用量子科学講座
山本誠一
用語解説
- ※注1
放射線によるエネルギーの付与は線量と呼ばれる物理量で表されます。放射線治療では照射する放射線の空間的な線量分布から1人1人の患者さんに最適な治療計画を立案します。
- ※注2
陽子線治療中に生じる陽電子放出核種の分布をPET装置によって画像化する試みは既に複数の治療施設で実施されています。その詳細については以下の論文を参照ください。
- ※注3
陽電子放出核種は陽電子を放出することで安定な原子核へと変化します。半減期とは陽電子放出核種の半数が安定な原子核になるまでの時間を表し、その値は核種毎に異なります。
本研究は、科学研究費補助金・基盤研究(S)(H27~31年度)「実用化へ向けた高解像度3Dカラー放射線イメージング技術の開拓」(代表:片岡淳:早稲田大学理工学術院・教授)、AMED先端計測分析技術・機器開発プログラム(H25~29年度)「粒子線治療における腫瘍の線量応答性観測システムの開発」(代表:西尾禎治:東京女子医科大学医学研究科・教授)の御支援を戴いて実施したものです。







