早稲田大学理工学術院の柴田重信教授の研究グループは、世界で初めて1個体のマウスの体内時計を生きた状態で測定する方法を開発しました。地球の自転に合わせて約24時間の周期で振動する時計遺伝子は体の中のあらゆる細胞で発現しており、様々な生理現象に「昼・夜」という情報を伝える重要なシステムを担っていますが、実際の生体内では組織や臓器の時計の時間合わせの能力がどれくらい機能しているのかは疑問でした。同研究グループは時計遺伝子の下流にホタルルシフェラーゼ遺伝子を導入したマウス(PER2::LUCマウス)と高感度EMCCDカメラを搭載したin vivo imaging装置(IVIS® Kinetic、Caliper社)を用いて、1個体のマウスの体内時計を生きた状態で測定しました。また、マウスの末梢組織の体内時計を脳内にある視交叉上核と呼ばれる小さな神経核が制御していることも確認しました。なお、この成果についてはCurrent Biology誌のオンライン版に掲載されました。
1.研究の背景

地球上の生物は地球の自転に合わせて24時間の生活リズムを刻んでおり、そのメカニズムとして約24時間の周期で振動する時計遺伝子の存在が近年明らかにされてきました。時計遺伝子(Per2, Bmal1)は体の中のあらゆる細胞で発現しており、様々な生理現象に「昼・夜」という情報を伝える重要なシステムを担っています。我々哺乳類の体内時計は、脳にある視交叉上核と呼ばれる小さな神経核が主時計として体の臓器や組織の末梢時計を調節していると考えられてきました。ところで培養した組織や細胞を用いた研究により、体外で培養している細胞も独自に時間を合わせる能力がある事が近年分かってきました。しかし、実際の生体内では組織や臓器の時計の時間合わせの能力がどれくらい機能しているのかは疑問でした。
マウスを用いた生体内(in vivo)での体内時計研究は、上述の生体外(in vitro)での研究結果を発展させるのに必須であり、また臓器間の時計の相互関係を調べるのには必須の技術であり、in vivoでの体内時計測定法の開発は待ち望まれていました。そこで今回我々は、時計遺伝子の下流にホタルルシフェラーゼ遺伝子を導入したマウス(PER2::LUCマウス)と高感度EMCCDカメラを搭載したin vivo imaging装置(IVIS® Kinetic、Caliper社)を用いて、世界で初めて1個体のマウスの体内時計を生きた状態で測定するユニークな方法を開発しました。この方法はとても簡便であり、また実験誤差が少なく、動物倫理的にも優れた方法です。(研究概要イメージ、図1)
2.研究手法と成果
(1)体内時計測定法の確立
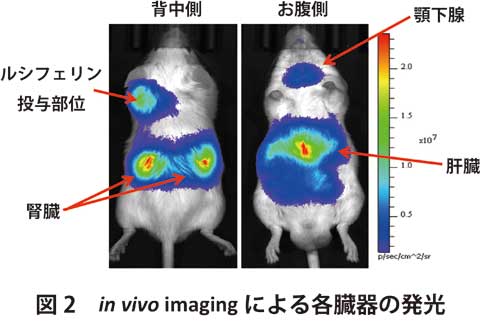
時計遺伝子Per2の下流にホタルの発光酵素であるルシフェラーゼ(Luciferase)を導入したマウスは、PER2::LUCEFERASEという複合タンパク質を生成します。発光基質であるルシフェリンをこのマウスに投与する事で、PER2::LUCIFERASEの量に相関した生物発光が各臓器で見られます。この発光はとても微量ですが、暗闇の中で高感度EMCCDカメラを用いて撮影する事で、皮膚から透過した光として臓器の発光を測定する事が出来ます(図1)。我々は、この撮影を4時間おきに24時間連続で行う事で、 図2のような綺麗な発光リズムを得る事に成功しました。また、もう一つの時計遺伝子であるBmal1はリズムのピーク時刻がPer2と逆の時間になる事が知られています。このBmal1に発光システムを導入したマウス(Bmal1-ELucマウス)で同じ手法を用いることで、発光リズムが逆位相になる事も示しました。
(2)視交叉上核を破壊したマウスの体内時計を測定
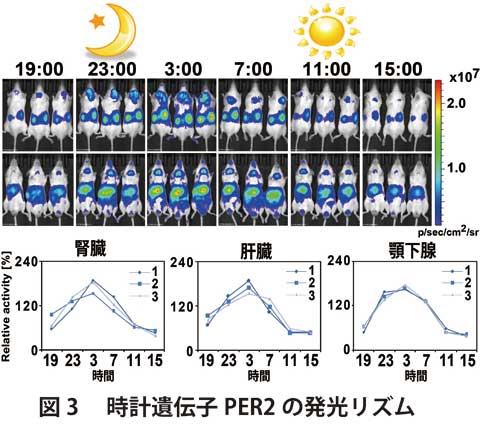
体内時計の中枢と考えられてきた視交叉上核を熱破壊したマウスは、行動、睡眠・覚醒リズムが消失しました。我々はそのマウスの末梢組織の肝臓・腎臓・顎下腺の体内時計を測定したところ、振幅が有意に減弱している事から、マウスの末梢組織の体内時計を視交叉上核が制御している事を発見しました。また、破壊したマウスの一部は破壊一ヶ月後でも、時計が止まることなく、振幅が落ちた小さな時計として維持していることが分かりました。その時計のリズム周期(約23.7時間)は臓器間で差異が無く、恒暗条件下での行動リズムの周期と同じであることから、主時計も末梢時計も似た分子機構で時計を刻んでいる可能性が示唆されました。
3.今後の期待
in vivoでの生物発光測定は癌研究で近年積極的に取り入れられてきていますが、まだ手法への疑問点も残っています。今回我々は、多くの基礎的な実験結果と共に新しく体内時計を正確に簡便に測定する方法を確立しました。今後の研究課題として生体内での研究は必須項目であり、我々の手法を用いた新しい発見、また他の分野での応用・発展に期待したいと考えています。
末梢組織の体内時計は代謝や免疫や癌の発症など多くの重要な機能に関わっています。リズム障害者(睡眠障害や交代勤務者)の代謝、免疫機能の悪化は疫学調査等で明らかにされています。今回、我々は脳にある主時計が働かない状態を物理的に作り出す事で、体内時計を評価しました。今後の研究として、リズム障害モデルマウスを用い、疾病や薬物治療における末梢体内時計の役割解明に今回の技術を応用したいと考えています。
論文題名及び著者
Current Biology:In Vivo Monitoring of Peripheral Circadian Clocks in the Mouse
田原 優1、3、黒田 大暁1、齋藤 恵祐1、中島 芳浩2、久保 祐二1、大西 信明1、瀬尾 泰裕1、大塚 槙子1、布施 悠太1、大浦 雄紀1、小松 拓矢1、森谷 洋平1、岡田 慧1、古谷 直樹1、平尾 彰子1、堀川 和政1、工藤 崇3、柴田 重信1
(1早稲田大学理工学術院・先進理工学研究科、2産業技術総合研究所・健康工学研究部門・生体機能制御研究グループ、3Department of Psychiatry and Biobehavioral Sciences, University of California-Los Angeles)
リンク
In Vivo Monitoring of Peripheral Circadian Clocks in the Mouse

