
タンパク質は折りたたまれて機能する
生命の担い手であるタンパク質はアミノ酸が連なったひも状の高分子で、特有の形に折りたたまれ、立体構造をとることで機能します。合成されたばかりのアミノ酸のひもは不安定なので、「分子シャペロン」と呼ばれるタンパク質がくっつき、正しく折りたたまれるように手助けしています。
分子シャペロンの多くは熱ショックタンパク質(Hsp)で、細菌からヒトまですべての細胞に普遍的に存在し、分子量によって、Hsp60、Hsp70、Hsp90などに分類されています。Hspは、細胞が熱などのストレスに曝されると、発現が上昇します。ストレスによって細胞内に変性したタンパク質が蓄積すると、正常な生理機能が維持できなくなるので、Hspがたくさんできて変性したタンパク質に結合し、正しい構造に戻して細胞を守っているのです。しかし、がん細胞では、Hsp70はがんの進展や悪性化に関与しています。
このような違いは、Hsp70の相互作用の相手が異なることによって生まれると考えられます。そこで、私たちは、細胞がさまざまなストレスを受けたときにHsp70が相互作用するタンパク質を見つけ、それを解析すれば、がん細胞のストレス応答機構をタンパク質レベルで明らかにできるのではないかと考えました。
大腸がん細胞の生存を助けるストレス応答因子
Hsp70には構造や機能が似た多くの種類がありますが、その仲間であるHsc70を使って実験することにしました。
この実験では血清飢餓(細胞に栄養を与えない)と、抗がん剤投与という2種類のストレスをがん細胞に与えました。その結果生じたHsc70複合体を解析したところ、血清飢餓ストレスを与えたときは、細胞内でタンパク質輸送に関わるタンパク質がHsc70と多く結合しており、抗がん剤ストレスでは代謝に関与するタンパク質が多く結合していました。私たちの予想通り、ストレスに応じてHsc70と結合するタンパク質は異なっていたのです。
そこで、次に、Hsc70と結合するタンパク質の働きを調べることにしました。2種類のストレスに共通して見つかった10種類の結合タンパク質のうち、Rab1Aがストレス応答に重要であることが、以下の実験からわかりました。まず、Hsc70の発現を抑えて、ストレスを与えると、Rab1Aは分解され、がん細胞は死んでしまいました。次に、Rab1Aの発現を抑えると、細胞が死んでしまったことから、Rab1Aはがん細胞の生存に必要な分子であり、Hsc70はRab1Aが分解されるのを抑えることで、がん細胞の生存を助けていることが示唆されました。
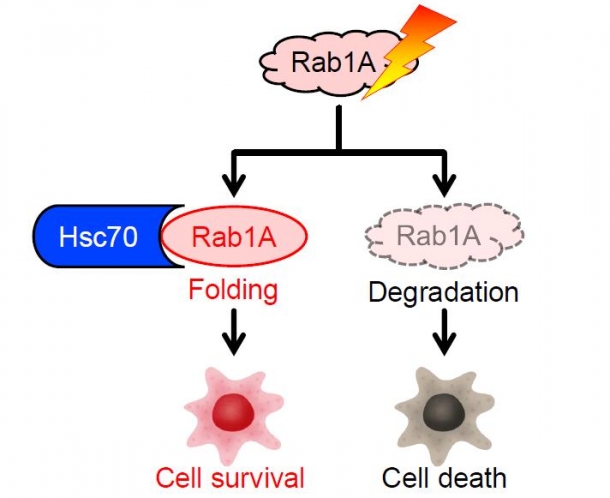
図1 Hsc70とRab1Aによるストレス応答
Hsc70はRab1Aを安定化させ、ストレス抵抗性を生じさせる。Hsc70が作用しないと、Rab1Aが分解され、がん細胞は死んでしまう。
スキルス胃がんの抗がん剤耐性
がんの治療では、抗がん剤を繰り返し使うと効きにくくなり、「抗がん剤耐性」として知られています。これも、抗がん剤というストレスに対して細胞が抵抗性を獲得する現象ですから、Hsp70と相互作用するタンパク質の解析によって、この機構を解明できるかもしれないと考えました。
対象としたのは、治療が難しいことで知られるスキルス胃がんです。がんがみつかったときには、外科治療が困難な場合も多く、化学療法に頼らざるを得ません。近年、このような切除不能な進行性、再発性の胃がん治療にはオキサリプラチンという抗がん剤が適応承認されましたが、耐性が生じることが問題になっています。耐性を獲得させた細胞は、オキサリプラチンに対する感受性が失われており、オキサリプラチンを投与した際の生存率が、もとのがん細胞に比べて高くなります。この耐性スキルス胃がん細胞から複数のHsp70結合タンパク質を見つけ、それらの作用を解析した結果、「SDF-2」を新たな耐性因子として同定することができました。
さらに、耐性スキルス胃がん細胞において、SDF-2遺伝子の働きを抑え、SDF-2タンパク質がつくられないようにすると、オキサリプラチンに対する感受性が高まり、生存率が低下しました。耐性が生じても、SDF-2が働かなければ、オキサリプラチンに対する感受性が高まり、再び効くようになるのです。
耐性細胞と薬が効く感受性細胞を比べると、耐性細胞のほうが、SDF-2タンパク質のレベルが高い(つまり、安定に存在している)ことがわかりました。このことから、スキルス胃がん細胞がオキサリプラチン投与によるストレスを受けると、Hsp70がSDF-2と結合して安定化させ、耐性を生じさせていると考えられました。このメカニズムから、SDF-2タンパク質を薬剤のターゲットにすれば、オキサリプラチン耐性を制御できる新たな治療法につながると期待しています。
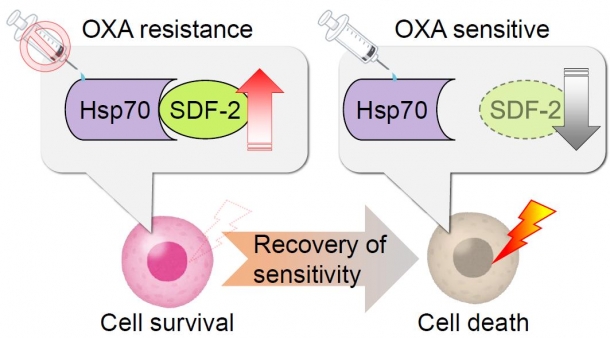
図2 Hsp70 によるオキサリプラチン耐性
Hsp70 がSDF-2に結合し、安定化させることでスキルス胃がん細胞はオキサリプラチンに対する耐性を獲得する。
Hsp70との相互作用を利用した解析法は、従来のタンパク質合成や遺伝子発現を利用した解析法とは異なり、ストレスの種類に応じて、応答に関わるタンパク質を網羅的に見つけることのできる画期的な方法です。ここでは、がん細胞の例を取り上げましたが、この方法は、さまざまな細胞に幅広く応用可能であり、がん以外の病気の治療法開発や、生物現象の理解にも貢献するものです。今後は、この方法をさらに発展させたいと考えています。
取材・構成:佐藤成美
協力:早稲田大学大学院政治学研究科J-School










