
進化するがん治療法
2018年のノーベル医学生理学賞を受賞された本庶佑先生は、がん細胞を攻撃する免疫細胞にブレーキをかけるタンパク質「PD-1」を発見し、それを画期的ながん免疫療法に結びつけました。いまや免疫療法は、手術、放射線治療、抗がん剤治療に続く第四の治療法となっています。
新しい治療法が登場する一方で、進行がんは転移を起こしたり、薬剤耐性を獲得したりして治療が困難です。また仮に早期発見しても、すい臓がんのような難治性のものもあります。こうしたがんを克服するには、“そもそもがんにならない”ことが重要だと私は考え、「がんの予防的治療法」の確立をめざすようになりました。
私たちの体に備わった“がんにならないためのメカニズム”
私たちの体の中では毎日のように、遺伝子に変異が入り変異細胞が生じています。しかし、変異細胞ががんにまで成長することはほとんどありません。それは、変異細胞を排除する仕組みがあるからです。その代表は、免疫細胞による変異細胞への攻撃です。
変異細胞を排除する仕組みとして、正常な上皮細胞が変異の入った上皮細胞を押し出すという仕組みも、20年以上前から知られています(図1)。これは、異なる性質をもつ細胞同士が、限られた生息域内で生存を賭けて争った結果、適者(ここでは正常な上皮細胞)が残る現象で、「細胞競合現象」とよばれています。この仕組みがうまく働かないと、がんになるわけですが、詳しいメカニズムは明らかになっていませんでした。そこで、私はがんの予防的治療の開発のために、細胞競合現象のメカニズムを解明しようと考えました。
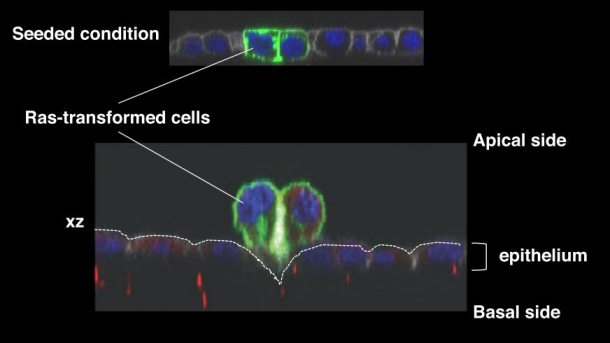
図1:Ras遺伝子に変異が入った変異細胞が正常の上皮細胞によって排除される様子を捉えた。
細胞競合現象を解明
多くのがんは、遺伝子変異がいくつも重なった結果生じます。最初に変異を起こす遺伝子の一つとして、Ras(ラス)が知られています。Ras遺伝子に変異が入った段階では、細胞はまだがん化していませんが、正常な上皮細胞はこの変異細胞を排除します。そこでRas遺伝子に変異が入った時、両方の細胞にどのような変化が起こるかを調べました。
Ras遺伝子に変異の入った変異細胞内では、正常細胞と接している側にミオシンが集積され、ほんの少し固くなることがわかりました(図2)。一方、変異細胞に隣接する正常細胞内では、変異細胞との境界面にフィラミンが集積され、このフィラミンが変異細胞を物理的に押し出す力となっていることが分かっています。また、変異細胞のミオシン集積が刺激となって、正常細胞のフィラミン蓄積が起こることも分かっているため、ミオシン集積を亢進させる物質を探索し、変異細胞を含む上皮細胞にこれを与えてやりました。予想通り変異細胞の排除を促すことがわかりました。この物質の効果はマウスでも確かめられ、がん予防薬の候補と考えられますが、毒性が強いという問題があり、これから解決しなくてはなりません。
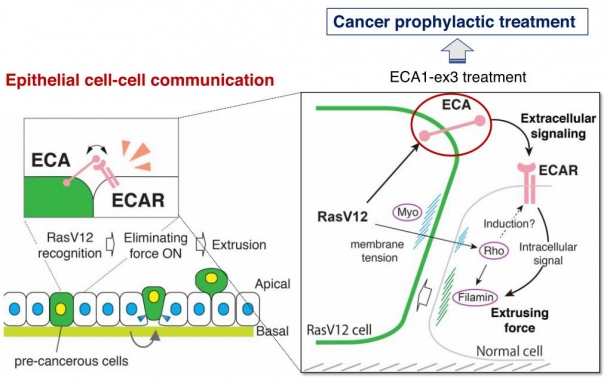
図2:上皮細胞表面に新たに発見されたECAとECAレセプター。
さらに研究を進めると、上皮細胞にRas遺伝子の変異が入ったとしても、正常の上皮細胞に囲まれていなければミオシンの集積が起こらないことが明らかになりました。この事実は、変異細胞と正常細胞の間で何らかのコミュニケーションが行われていることを示しています。私は以前から、免疫系で樹状細胞が抗原を提示することでT細胞、B細胞とコミュニケーションを図る仕組みをとても美しいと思っていました。そこで、上皮細胞の細胞競合現象でも、免疫細胞と同様の仕組みが働いているのではないかと予想しました。
この予想は当たり、変異細胞の表面には、免疫系の抗原に相当する「上皮抗原関連タンパク質 (epithelial antigen-associated protein; ECA)」が、正常細胞の表面にはそれを認識するECAレセプター(ECAR)があることを発見したのです。さらに、ECAの細胞外ドメイン(ECARに結合する部分)を添加したところ、正常細胞でのフィラミンの集積が亢進しました。これらのことから、変異細胞のつくるECAが、ECARを介して正常細胞のフィラミン蓄積を促していると結論付けました。
多くの医療分野に応用される可能性
細胞間コミュケーションのメカニズムが明らかになるにつれ、製薬会社もそれを応用した「がんの予防的治療」に興味を持ち始めています。そうした流れの中で、私自身も細胞間コミュケーションの真実に迫ろうとしているという実感があり、研究はとても楽しいです。今回の成果を、健康食品のように日々の生活の中で気楽に摂取できるがん予防薬に発展させたいと考えています。
細胞間コミュニケーションが関与する疾患は、がんだけに限りません。例えば、ウイルスに感染した細胞を排除するときにも、感染細胞と非感染細胞間のコミュニケーションが関わっているでしょう。また、移植細胞が周辺の細胞から押し出されて生着できなかったり、アルツハイマー病で神経細胞が破壊されたりする現象にも細胞間コミュニケーションが関与していると考えられています。細胞間コミュニケーションの研究が進み、多くの疾患の治療につながることが、私の願いです。
取材・構成:池田亜希子
協力:早稲田大学大学院政治学研究科J-School










