- 枝川 義邦(Yoshikuni Edagawa)准教授(2010年3月当時)
ミクロ薬理学という概念~逆転の発想
薬理学という学問は、生物に薬物を投与して、その個体、もしくは組織がどのような応答をするかという点を理解するためのものです。つまり、細胞の集合体を構成する全体がどのような影響を受けているかという分析を行っています。これに対して、私は「ミクロ薬理学」という言葉を作りました。ミクロ薬理学のコンセプトとは、細胞内のより微細な構造、一部分だけに薬物を投与したものが、細胞全体、ひいては細胞の集団にどのように作用していくかということを解析するというものです。これまでの「全体から部分へと」向かう薬理学の研究の流れを「部分から全体へ」と逆転させたわけです。英語では、「ミクロ薬理学」に “micropharmacology”という言葉をあてますが、実はこれも細胞や組織に作用させた薬物が細胞内の微細構造に及ぼす影響を見ているものばかりですので、ここで言うミクロ薬理学のコンセプトとは違っています。
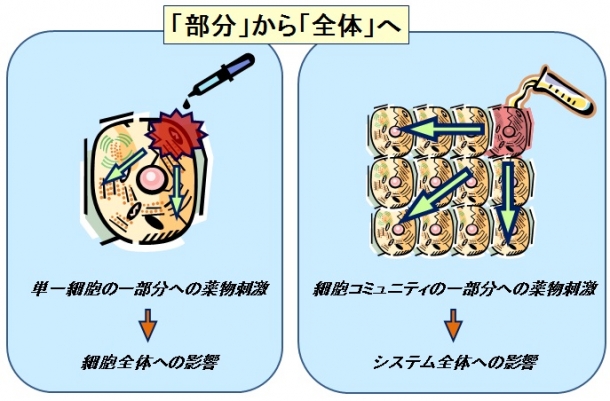
図1 ミクロ薬理学のイメージ。細胞やコミュニティの一部分への薬物刺激が、全体へと及ぼす影響を分析するものである。(提供/枝川義邦准教授)
細胞には「個性」がある
例えば人間の体は60兆個もの細胞からなり、性質が似ている細胞が集まって臓器や組織を構成しています。細胞一つ一つの性質は、細胞の形、どのような物質やタンパク質を作り分泌するかという細胞の機能、そして薬物への応答性などの違いがあります。たとえ同じ種類の細胞で、同じゲノムをもっていたとしても、個々のもつ性質は異なっているのではないかと考え、その一つ一つの細胞がもつ「個性」に着目しました。それを解明するのがこの研究のコンセプトです。これまでにも、1種類の細胞が分裂を繰り返していくうちに、同じ環境においても機能が異なってくるという報告があります。また、私の研究でも、同じ性質の細胞を培養してできた細胞群のうち、群れの内側にある細胞と、外側にある細胞とでは違う役割を果たしているという発見もありました。そこで、分析化学の分野で注目されているマイクロTAS(Total Analysis System)と呼ばれる微小デバイスを用いて一つ一つの細胞の性質を調べることを考えました。
手のひらの上の研究室~マイクロTAS
通常の細胞生物学の研究室では、生体から細胞を取り出す→ターゲットとなる細胞を分離→培養→分析もしくは細胞内因子を分離した上での解析、という一連の工程を大がかりな装備を用いて行っています。マイクロTASとは、そのすべての工程を、半導体分野の微細加工技術を応用して作った微小なチップの中で行おうというコンセプトです。昔は巨大だったコンピュータが、今は小さなCPUになってパソコンの中に入っているのと似ています。このようなマイクロTASのアイデアを細胞生物学の研究に応用しようとする発想はかねてよりありましたが、すべての過程を可能にするシステムの実現は困難でした。ですが近年では、このようなコンセプトを叶える装置を作ることが可能になってきました。
我々が使っているマイクロ流体システム(図2)はその中の一つです。マイクロ流体デバイスに刻まれた経路に、均一な細胞が多数存在する懸濁液を流すことにより、細胞を傷つけずにとらえることができます。細胞の捕獲だけでなく、細胞をそのまま培養し解析したり、薬物を投与することもできます。このデバイスはPDMS(ポリジメチルシロキサン)という高分子素材で作製されており、透明で細胞の観察が容易であり、毒性がないことが利点です。マイクロ流体デバイスには、経路に培養液や薬物を流すためのポンプがつながれています。蛍光顕微鏡、CCDカメラがデバイス内の一連の反応をとらえます。
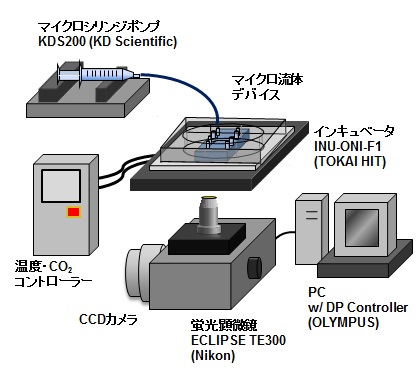
図2 マイクロ流体システムの構成。デバイスはインキュベータの上に置かれ、適温に調整することで細胞の捕獲と培養、反応がシステム内で行われる。(提供/枝川義邦准教授)
マイクロ流体デバイスのミクロ薬理学への応用
マイクロ流体デバイスの実際のイメージは、図3のようになっています。これはデバイスを上から見たところです。直径が35㎜の細胞培養皿を使ったデバイスの中に、液体を通す3本の経路があります。各々の経路はマイクロメートルオーダー幅で、それぞれの経路は幅3μmの小孔でつながれています。細胞が流れる経路にはキャプチャーポケットと呼んでいる半円筒状の凹みがいくつも並んでいます。細胞が多数含まれている懸濁液を一つの経路に流し、残りの経路には培養液を流します。各々の経路を流れる液体の速さを調節することにより、細胞は凹みにうまく入り込み、捕獲されます。
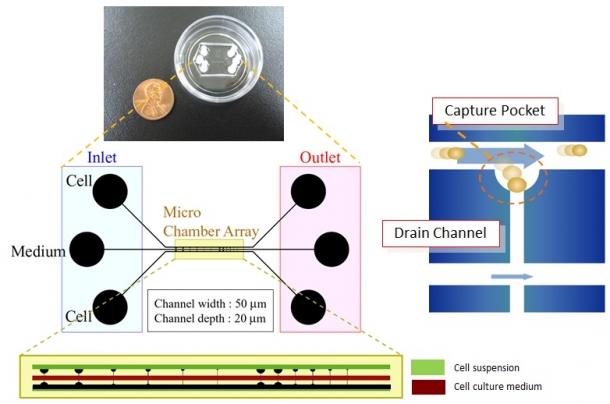
図3 マイクロ流体デバイスのデザイン。細胞と培養液が流れる3経路の中央にあるマイクロチャンバーアレイで細胞が捕獲される。右は、細胞捕獲のしくみ。(提供/枝川義邦准教授)
この経路の優れているところは、その物理的な特性を活かして、細胞の一部に薬液を暴露させることができるところです。マイクロ流体デバイス内で組成の違う液体が多方向からやってきて合流すると、互いに混合されず安定した界面を作り、層流になります。その現象をミクロ薬理学へ応用して、界面に近い細胞だけに薬物を反応させたり、細胞の一部分や細胞コミュニティのきわめて限られた部分だけに投与することができるようになりました。例えば、隣接する2つの細胞のうち片方の細胞だけのミトコンドリアを染色し、その拡散を観察するとか、細胞のある部分のみ薬液に反応させるといったことが可能になりました。このように、マイクロ流体システムを用いて、単一の細胞やコミュニティの局所的な変化がいかに全体に影響を及ぼすかという分析研究を重ねることにより、ミクロ薬理学の発展、ひいては細胞一つ一つの特異性を見いだす細胞「個性」の理解へとつながっていくものと期待しています。
取材・構成:青山聖子/大山聡美
協力:早稲田大学大学院政治学研究科J-School










